ワイエムシィでは、核酸、ペプチド、タンパク質分離用に、イオン交換、サイズ排除、疎水、逆相の4種のモードの製品をラインナップしています。
チャージバリアントなど荷電状態が異なる成分の分離には、イオン交換が用いられます。疎水性の異なる生体分子を、活性を維持したまま分離するには疎水クロマトグラフィーが有効です。ペプチドマッピングなどの特性解析には逆相が、分子量が大きく異なる抗体とその凝集体やフラグメントの分離などにはサイズ排除が適しています。
分離の用途や目的によって、適切な分離モードを選択することで、迅速な検討が可能です。
| モード | イオン交換 | サイズ排除 | 疎水 | 逆相 |
|---|---|---|---|---|
| 対応製品 | Accura BioPro IEX BioPro IEXカラム |
YMC-SEC MAB YMC-Pack Diol |
BioPro HIC HT | YMC-Triart (バイオ クロマトグラフィー用) |
| 分離の原理 | 電荷 | 分子サイズ | 疎水性 | 疎水性 |
| 適用分子量 | 数百万まで | 約100万まで | 数百万まで | 約15万まで |
| 分離能 | +++ | ++ | +++ | +++ |
| スピード | ++ ~ +++ | + | +++ | +++ |
| 試料負荷量 | +++ | ++ | +++ | ++ |
| 試料安定性 | +++ | +++ | +++ | + ~ ++ |
| 用途 | チャージバリアント分析 | 凝集体分析 フラグメント分析 |
抗体薬物複合体の 薬物結合数分析 |
ペプチドマッピング LC-MS 構造解析 |
イオン交換では、各化合物の電荷の差を利用して試料の分離を行います。固定相にはイオン解離基を持つアニオン交換体、カチオン交換体を使用し、移動相には緩衝液にカウンターイオンを添加して使用します。イオン結合により、担体にタンパク質などの化合物を結合させ、移動相中のカウンターイオンの濃度を高めていきます。カウンターイオン濃度を高めることでイオン結合が弱くなり、総電荷の小さい化合物から溶出します。
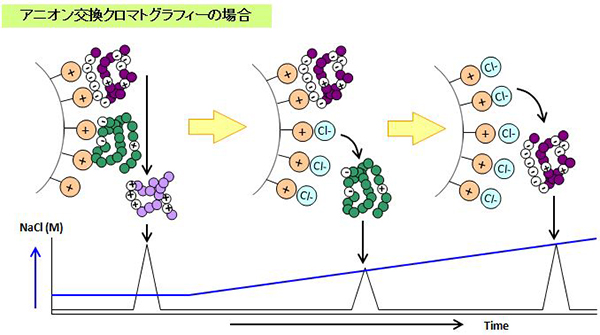
タンパク質のチャージバリアント分析には、一般的にイオン交換クロマトグラフィーを用います。
陽イオン交換カラムBioPro IEX SFで4種のモノクローナル抗体をpHグラジエントモードおよび塩グラジエントモードで分析した結果、どちらのモードにおいてもシャープなピーク形状が得られ、チャージバリアントの多くのピークやアイソフォームの分離が確認できました。
| 1. natalizumab |
| 2. cetuximab |
| 3. adalimumab |
| 4. denosumab |
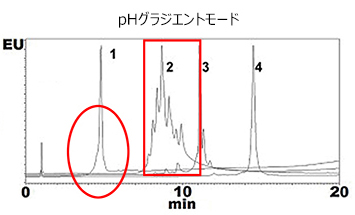
| Column | BioPro IEX SF (5 μm), 100 X 4.6 mmI.D. |
|---|---|
| Eluent | A) CX-1 pH Gradient Buffer A* (pH 5.6) B) CX-1 pH Gradient Buffer B* (pH 10.2) 0-100%B (0-20 min) |
| Flow rate | 0.6 mL/min |
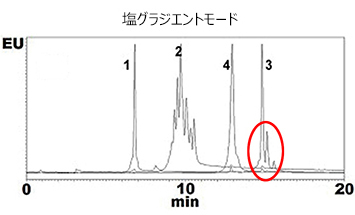
| Column | BioPro IEX SF (5 μm), 100 X 4.6 mmI.D. |
|---|---|
| Eluent | A) 10 mM MES-NaOH (pH 5.7) B) 10 mM MES-NaOH (pH 5.7) containing 1 M NaCl 0-20%B (0-20 min) |
| Flow rate | 0.6 mL/min |
サイズ排除クロマトグラフィーは、分子サイズによって分離する手法です。固定相には網目構造の細孔を有するシリカゲルやポリマーを使用し、化合物の溶解性や安定性が高いpHの緩衝液を移動相に用います。化合物は細孔の内部深くまで入り込む小さい分子ほど溶出が遅く、細孔の内部に入りにくい大きい分子ほど早く溶出されます。
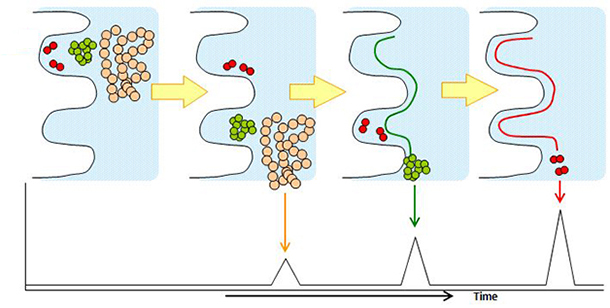
タンパク質の単量体(モノマー)、二量体、凝集体や分解物の分離には、サイズ排除クロマトグラフィーが用いられます。
抗体分離用に最適化されたYMC-SEC MABでは、モノマーと凝集体のピークが十分に分離できました。また、タンパク質分解酵素パパインで断片化したモノクローナル抗体の分析においては、同等の分子量であるFcとFabも分離良好でした。
モノクローナル抗体と凝集体の分析
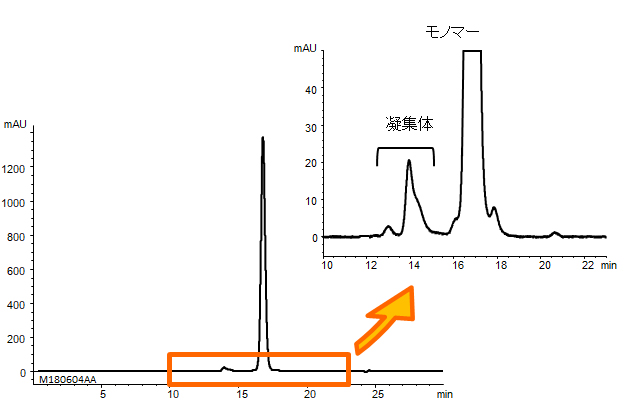
| Column | YMC-SEC MAB (3 µm, 25 nm) 300 X 4.6 mmI.D. |
|---|---|
| Eluent | 0.1 M KH2PO4-K2HPO4 (pH 7.0) containing 0.2 M NaCl |
| Flow rate | 0.165 mL/min |
| Temperature | 25ºC |
| Detection | UV at 280 nm |
| Injection | 10 µL (5 mg/mL) |
| Sample | Humanized monoclonal antibody |
フラグメントの分析
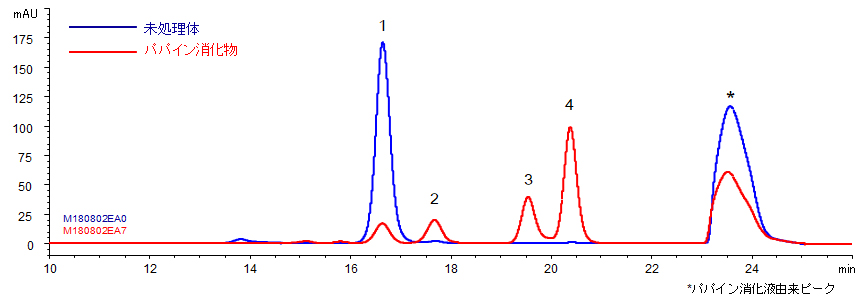

| Column | YMC-SEC MAB (3 µm, 25 nm), 300 X 4.6 mmI.D. |
|---|---|
| Eluent | 0.1 M KH2PO4-K2HPO4 (pH 7.0) containing 0.2 M NaCl |
| Flow rate | 0.165 mL/min |
| Temperature | 25ºC |
| Detection | UV at 280 nm |
| Injection | 2 µL (3 mg/ml) |
| Sample | Humanized monoclonal IgG1 + Papain消化液 |
疎水クロマトグラフィーは、担体とタンパク質などとの疎水性相互作用を利用して分離します。逆相とは異なりリガンドの導入率が少なく、移動相に有機溶媒ではなく硫酸アンモニウムを使用するため、タンパク質の変性がなく活性を維持したままでの分離が可能です。移動相の硫酸アンモニウムの濃度を下げることでリガンドとの結合力が弱まり、タンパク質が溶出します。
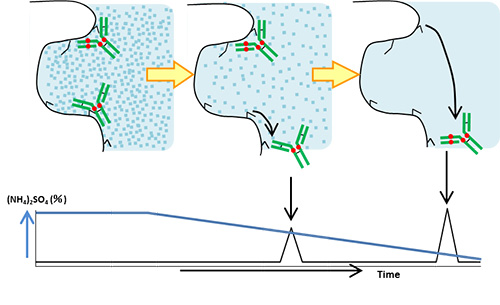
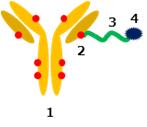
モノクローナル抗体に低分子薬物(ペイロード)を結合した抗体薬物複合体(Antibody-drug conjugate; ADC)は、その薬物の結合数(Drug to Antibody Ratio; DAR)によって疎水性が異なるため、疎水クロマトグラフィーによって分離できます。
BioPro HIC HTを用いたADCのDAR分析では、良好な分離が得られました。
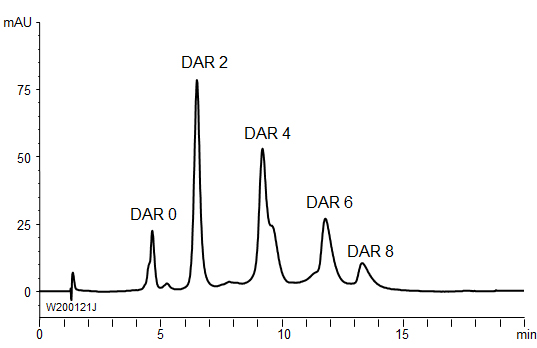
| Column | BioPro HIC HT (2.3 μm), 100 X 4.6 mmI.D. |
|---|---|
| Eluent | A) 20 mM NaH2PO4-Na2HPO4 (pH 7.0) containing 1.0 M (NH4)2SO4 B) 20 mM NaH2PO4-Na2HPO4 (pH 7.0)/2-propanol (90/10) 0-100%B (0-15 min), 100%B (15-20 min) |
| Flow rate | 0.5 mL/min |
| Temperature | 25ºC |
| Detection | UV at 280 nm |
| Injection | 10 µL |
| Sample | Brentuximab vedotin (2.5 mg/mL) |
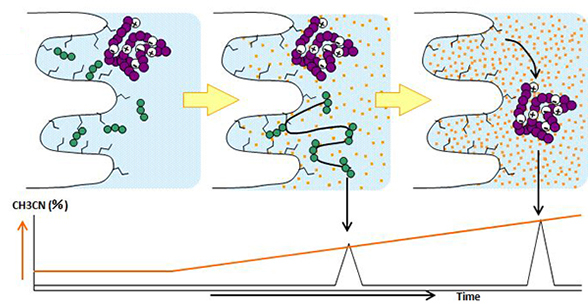
逆相クロマトグラフィーは、化合物と固定相・移動相との疎水性相互作用によって分離させる手法です。シリカゲルや有機シリカハイブリッドなどの基材にC18、C8、C4などの疎水性官能基を化学結合させた固定相を用い、移動相には酸水溶液や緩衝液などと有機溶媒の混合溶液を用います。移動相の有機溶媒比率を高めていくと疎水性の小さい化合物から順に溶出します。
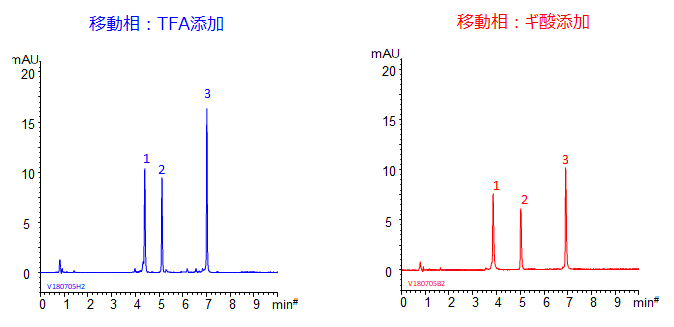
逆相クロマトグラフィーは、高分解能・高分離能で、MSと組み合わせやすい利点があり、抗体の分解物やフラグメントの分析、ペプチドマッピングにおいて利用されます。LC-MSでは高感度が期待されるギ酸添加の移動相が好まれますが、ピーク形状が不良になりがちです。YMC-Triartカラムではギ酸添加の条件でも良好なピーク形状が得られました。
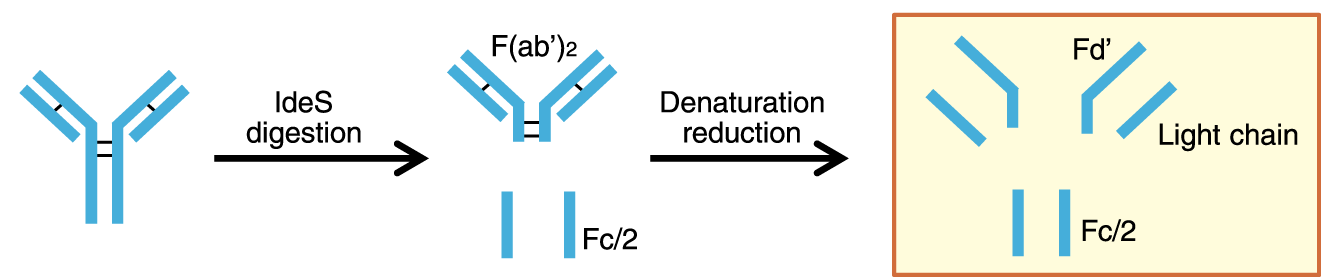
| Column | YMC-Triart Bio C4 (1.9 µm, 30 nm), 150 X 2.1 mmI.D |
|---|---|
| Eluent <TFA> | A) water/TFA (100/0.1) B) acetonitrile/TFA (100/0.1) 25-50%B (0-10 min), 90%B (10-12.5 min) |
| Eluent <Formic acid> | A) water/formic acid (100/0.1) B) acetonitrile/formic acid (100/0.1) 20-45%B (0-10 min), 90%B (10-12.5 min) |
| Flow rate | 0.4 mL/min |
| Temperature | 80°C |
| Detection | UV at 280 nm |
| Injection | 4 µL (0.25 mg/mL) |